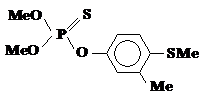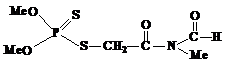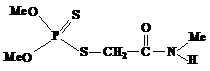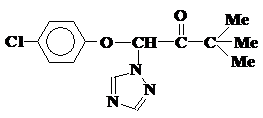4.2.5. Трансформация пестицидов в живой природе
Многие пестициды участвуют в одно- и многостадийных химических превращениях непосредственно в живых организмах. Далеко не все продукты этих превращений безвредны.
Проникая в организм животного через дыхательные пути, наружные покровы, кишечный тракт, пестициды претерпевают двоякие изменения [76]:
- химические превращения – окисление, восстановление, гидролиз,
- комплексообразование, т.е. образование комплексных соединений (конъюгатов) с биохимическими компонентами организма.
Процессы химических превращений контролируются с помощью энзимов (биологических катализаторов), которые содержатся в печени и в меньшей степени в кишечнике, почках, железах и т.д. Примеры некоторых энзиматических систем представлены в табл.4.3.
Химические превращения пестицидов необратимы, тогда как при комплексообразовании возможно последующее высвобождение пестицида в первоначальном виде.
Обратимся к превращениям ХОП.
Инсектицид гептахлор (ЛД50 для мышей составляет 82 мг/кг [12]) в живых организмах окисляется в эпокси-продукт, который практически для всех видов организмов вдвое более токсичен по сравнению с исходным [18, 74].
Инсектицид альдрин (ЛД50 = 40-50 мг/кг) в растениях, организме насекомых и позвоночных, а также в почве окисляется в протравитель семян дильдрин (ЛД50 = 25-50 мг/кг), который столь же опасен для людей [19].
Альдрин Дильдрин
Особенно разнообразны и опасны превращения ФОП, попавших в живые организмы.
В качестве примера приведем биотрансформацию инсектицида и акарицида широкого спектра действия дикротофоса (бидрина). В процессе этого превращения образуются два продукта – монокротофос (азодрин) и его амидный аналог, причем оба оказываются тератогенными веществами [1].
Таблица 4.3. Энзиматические системы живых организмов, осуществляющие химические превращения пестицидов [74]
|
Энзимы |
Место в организме |
Метаболизируемые пестициды |
|
Первое направление метаболизма |
||
| Оксидазы смешанной функции | Микросомы, печень позвоночных и жир насекомых. | Многие липофильные пестициды. |
| ДДТ-дегидрохлориназа | Имеется у насекомых и позвоночных животных. | ДДТ и ДДД. |
| Эпоксид гидраза | Микросомы, особенно печени млекопитающих. | Дильдрин и эпоксид гептахлора. |
|
Второе направление метаболизма |
||
| Глюкоронил трансферазы | Микросомы, особенно печени, коры надпочечников и кишечного тракта. Распространены у позвоночных, кроме рыб, и у насекомых. | Многие пестициды с подвижным хлором, включая метаболиты дильдрина. Хлорфенвинфос. |
| Глутатион-s-трансферазы | Печень позвоночных животных. | Многие ХОП, в том числе гамма-ГХЦГ и тетрахлорнитробензол. |
С неожиданными поворотами развивалась история вхождения в жизнь одного из ФОП - фунгицида афоса (1-ацетокси-2,2,2-трихлорэтил-О,О-дифенилфосфонат), с помощью которого предполагалось бороться с ржавчиной злаков на посевах пшеницы и риса. Он был изучен гигиенической наукой [204], которая заключила, что этот фунгицид не опасен, поскольку быстро разрушается в объектах окружающей среды [490]. Вскоре, однако, выяснилось, что при распаде в организме млекопитающих этот фунгицид образует еще более ядовитые вещества, чем исходное [491]. В связи с этим санитарно-эпидемиологическая служба была вынуждена в 1986 г. запретить афос – после многих лет применения [42].
Подобных примеров образования ядовитых веществ в результате метаболических превращений пестицидов в живых организмах известно сотни. Причем изученные примеры такого рода, несомненно, составляют лишь небольшую часть реально существующих. Табл.4.3, опубликованная еще в 1960 гг., дает некоторое представление об этом аспекте проблемы.
Таблица 4.3. Сравнительная токсичность пестицидов и их метаболитов (для крыс) [466]
|
Пестицид |
ЛД50, мг/кг |
Метаболит |
ЛД50, мг/кг |
Рост токсич-ности, раз |
| Меркаптофос |
7,7 |
Сульфоксид |
2,0 |
3,9 |
| Тиофос |
13,0 |
Параоксон |
3,0 |
4,3 |
| Фосфамид |
250-800 |
P=O - фосфамид |
30-55 |
~8-15 |
| Фосфамид |
250-600 |
Тиоловый эфирфосфат (при нагревании) |
100 |
2,5-6 |
| Хлорофос |
560-633 |
ДДВФ (дихлорфос, при нагревании) |
76-80 |
~8 |
| Гептахлор |
60-169 |
Эпоксид гептахлора |
34-88 |
~2 |
| Цирам |
1230 |
ТМТД |
400 |
3,1 |
Знание опасных последствий отравления ФОП пришло не сразу. Тем более не ожидалось, что в организме теплокровных многие ФОП будут сохранять свою активность в форме токсичных метаболитов.
В целом метаболизм ФОП протекает в двух противоположных направлениях.
Одно из них - это обычная детоксикация, т.е. распад до более простых и менее токсичных соединений.
Однако наряду и параллельно с детоксикацией многие ФОП превращаются в живых организмах в более активные антихолинэстеразные и более токсичные вещества. Этот тип превращения ФОП (токсификация, летальный синтез [49]) чрезвычайно важен для понимания пределов возможного их применения. И очень жаль, что об этом явлении не было в четкой форме сообщено в многочисленных общедоступных изданиях, например в известной академической и справочной монографии «Пестициды. Химия, технология и применение» [10]. Между тем знание этих особенностей, мягко говоря, не безразлично для тех, кто по различным причинам подвергся интенсивному воздействию ФОП.
Один из важнейших механизмов токсификации в ряду тионовых и дитиофосфорных эфиров является окислительная десульфурация, в процессе которой атом серы в связи P=S заменяется на атом кислорода (P=S Þ P=O). В результате этого непосредственно в живом организме возникают более токсичные ингибиторы холинэстераз.
Этот механизм усиления токсичности непосредственно в живых организмах был последовательно доказан для многих ФОП – тиофоса, метафоса, фосфамида, метатиона и т.д. При превращении метатиона в фенитрооксон токсичность возрастает за счет снижения ЛД50 с 420-516 мг/кг до 20 мг/кг [30]. В ряде случаев антихолинэстеразная активность ФОП возрастает очень значительно. В частности, для метафоса, карбофоса, тионового изомера меркаптофоса, как и у тиофоса, она повышается почти в 10 000 раз (данные получены еще в 1967 г.) [49]. В случае карбофоса наряду с превращением в более токсичный малаоксон происходит также образование токсичного изо-малатиона (см. выше).
Скорость процесса токсификации может быть различной. Например, при острой интоксикации человека системным инсектицидом сайфосом (меназоном) наблюдается скрытый период (до суток) и медленное нарастание антихолинэстеразного действия, что связано с превращением малоактивной PS-формы в активную PO-форму [165].
Еще один механизм превращения ФОП в организме теплокровных связан с их прямым окислением, сопровождающимся образованием более токсичных продуктов - сульфоксида и сульфона. В частности, это происходит в случае такого инсектицида контактного и кишечного действия, как байтекс (фентион, лебайцид) [18].
Байтекс
Особенно интересен случай превращения системного инсектицида и акарицида меркаптофоса (систокса), относящегося к числу СДЯВ и представляющего собой смесь изомеров (об этом ФОП см. также главу 11). При прямом окислении в организме человека сначала образуются соответствующие сульфоксиды (вследствие окисления этилмеркаптоэтильной части молекулы), превращающиеся затем в сульфоны. Сульфоксиды и сульфоны меркаптофоса обладают высокой антихолинэстеразной активностью и очень токсичны. Основной метаболит – сульфоксид тиолового изомера превращается в сульфон медленнее, чем сульфоксид тионового.
В дальнейшем продукты прямого окисления меркаптофоса претерпевают окислительную сульфурацию (при этом антихолинэстеразная активность сульфоксида и сульфона тионового изомера вновь повышается – в 3 и 6 раз соответственно) и лишь после этого гидролизуются до нетоксичных веществ [20, 49]. Эти данные, полученные в 1960 гг., в справочное издание 1987 г. [10] включены не были, хотя сам пестицид был запрещен к использованию в СССР еще в 1967 г. из-за больших людских потерь.
Приведем несколько примеров трансформации пестицидов в процессе реакций других типов.
Октаметил (шрадан) в организме человека и вообще теплокровных окисляется до фосфораминооксида. Окисленное соединение обладает более высокой антихолинэстеразной активностью [20]. Тем не менее этот ФОП был запрещен в СССР лишь в 1978 г. - почти через два десятилетия после начала производства.
Контактный и системный инсектицид антио подвергается в организме теплокровных не только окислению, но и восстановлению. В последнем случае образуется фосфамид - системный инсектицид и акарицид широкого спектра действия. Токсичность при этом возрастает с ЛД50 = 350 мг/кг до ЛД50 = 220 мг/кг [20, 30, 49].
В свою очередь фосфамид, как уже упоминалось, может подвергаться окислительной сульфурации с появлением продуктов еще большей токсичности.
Примером реакции дегидрохлорирования служит превращение в организме среднетоксичного инсектицида хлорофоса в высокотоксичный контактный инсектицид ДДВФ (дихлорфос, см. раздел 4.2.6) [20, 30, 49].
Продукты трансформации и метаболизма пестицидов в растениях могут обладать не только большей острой токсичностью, но и другими опасными свойствами. В частности, фталофос трансформируется с образованием фталимида и фталевой кислоты – веществ, обладающих тератогенным действием (фталимид вызывает уродства конечностей у новорожденных, чьи матери подверглись его воздействию) [18].
Превращения в более токсичные вещества непосредственно в живых организмах характерны не только для ФОП, ХОП, но и для пестицидов других классов.
Так, высокотоксичный акрекс, широко применяемый в тепличном хозяйстве в качестве акарицида контактного действия и фунгицида против мучнистой росы, в организме превращается в инсектицид и гербицид диносеб [17]. Токсичность возрастает при этом более чем в 2 раза (ЛД50 изменяется со 140 мг/кг до 60 мг/кг) [10].
Триадимефон (байлетон)
Метаболизм системного фунгицида триадимефона (байлетона) в грибах и растениях приводит к его превращению в смесь диастереомеров триадименола, фунгицидные свойства которого выше исходного продукта. В мицелии грибов процесс идет с большой скоростью, и содержание триадименола в мицелии в 20-30 раз превышает его концентрацию в других объектах окружающей среды. Такое превращение в равной степени протекает и в чувствительных к фунгициду резистентных грибах. В организме млекопитающих к этому процессу добавляется гидроксилирование трет-бутильной группы с последующим окислением до кислоты [10].
Инсектицид севин (карбарил, ЛД50 = 270 мг/кг), много десятилетий особенно широко применяемый в сельскохозяйственной практике, в растениях гидролизуется с образованием менее токсичных и менее стойких продуктов. Однако при окислительных процессах он трансформируется в 5-оксинафтил-N-метилкарбамат – вещество, столь же токсичное, как и сам севин (ЛД50 = 297 мг/кг) [10, 28].
Один из метаболитов фунгицида беномила (фундазола) – метиловый эфир карбаминовой кислоты (БМК, карбендазим) - также обладает фунгитоксическим действием. Карбендазим образуется в обработанных беномилом почве и растениях, где сохраняется длительное время [28].
В процессе превращения в растениях, в продуктах питания и просто в окружающей среде некоторые фунгициды дитиокарбаматного ряда, например цинеб, манеб и поликарбацин, образуют стойкие летучие метаболиты – этилентиомочевину, этилентиураммоносульфид. Токсичность метаболитов, как оказалось, в 2-10 раз выше токсичности исходных веществ. Продукты трансформации достаточно долго обнаруживаются в самих растениях, продуктах питания и воде (некоторые сохраняются в растениях и продуктах питания, например винограде, вишне и т.д., до двух месяцев, когда следы самих фунгицидов уже не обнаруживаются) [18, 28].
Гербицид атразин, а также производные триазина под влиянием растительных ферментов образуют вещества, обладающие более сильным мутагенным действием, чем исходные [66].
Приведенный перечень примеров, очевидно, далеко не полон. Однако и он вполне убедительно демонстрирует «богатство возможностей» опасных превращений пестицидов в живых организмах, с которым мы сталкиваемся и будем еще сталкиваться, когда бездумно вносим пестициды в нашу жизнь.
| « Назад | Оглавление | Вперед » |