ИСТОЧНИКИ ДИОКСИНОВ.
IV.1. Получение продукции
Ксенобиотики диоксинового ряда образуются при производственных процессах, целью которых является получение ароматических и алифатических хлор- и броморганических соединений, неорганических галогенидов. Образуются они и при выпуске иных химических продуктов с промежуточным использованием хлора, неорганических галогенидов, хлор- и броморганических соединений, в том числе в качестве катализаторов и растворителей.В работах [53,104,488] систематизированы лишь некоторые виды промышленных технологий, в процессе которых возможно по- путное генерирование диоксиновых соединений ПХДД и ПХДФ:
- - процессы производства хлорфенолов и их производных;
- - процессы производства хлорбензолов, ПХБ и их замещенных;
- - синтез хлоралифатических соединений;
- - процессы производства бромированных антипиренов (бифенилы, дифениловые эфиры и т.д.);
- - процессы с использованием хлорсодержащих интермедиатов;
- - процессы производства неорганических хлоридов;
- - процессы с использованием хлорированных катализаторов и растворителей, и т.д.
То же самое может относиться к некоторым процессам броморганической химии [104,488]. Кроме того, диоксины образуются в некоторых технологиях металлургической и целлюлозно-бумажной промышленности.
Следует подчеркнуть, однако, что каждое из существующих в мире хлорных и бромных производств может быть источником попутного образования диоксинов III-VIII лишь в принципе. Для ответа на вопрос о реальной опасности необходим специальный и последовательный анализ диоксиногенных характеристик всех существующих хлорных технологий.
Анализ технологий, которые обладают наибольшей опасностью для цивилизации, в особенности диоксиногенных технологий, проводится в промышленно развитых странах регулярно. Первое сравнительно полное рассмотрение подобного рода было осуществлено еще в 1980 г. в монографии [3]. В последние годы этому вопросу была посвящена серия работ [53,104,485,488,489].
Применительно к бывшему СССР проблема столь же актуальна, как и во всем мире [376,377,490]. Хлорорганический синтез занимает ведущее место в хлорной промышленности СССР. Как отмечалось в работе [491], по состоянию на 1985 г., например, около 80 цехов выпускали примерно 70 наименований хлорорганических соединений (не считая реактивов, промежуточных и побочных продуктов) с общим объемом 1,5 млн т в год. Тенденция роста этого направления промышленного производства была такова, что за период 1970-1985 гг. производство хлорированных продуктов увеличилось почти в 4 раза, а в перспективе их валовый выпуск предполагалось поднять до 3-3,5 млн т в год, в том числе хлорорганических пестицидов и других соединений. Эта тенденция действительно сохранялась. Во всяком случае к 1988 г. произошел заметный рост показателей, приведенных для 1985 г.: уже примерно 100 цехов производили 2 млн т хлорорганических продуктов. Соответственно росли и объемы вредных выбросов.
Максимальное внимание промышленности бывшего СССР к наращиванию объемов хлорных производств сопровождается, однако, лишь минимальным интересом к возможным последствиям этого процесса для живой и неживой природы. В связи с этим обсуждение проблемы источников диоксинов в нашей стране неизбежно сводится к анализу самих технологий и выявлению из них потенциально наиболее опасных. Это связано с тем, что по разным причинам обычно авторы не акцентируют внимание на диоксиновой проблеме (см., например, [366-370]). В качестве редкого исключения можно указать работу [492].
IV.1.1. Производство полигалогенфенолов, полигалогенанилинов и их производных
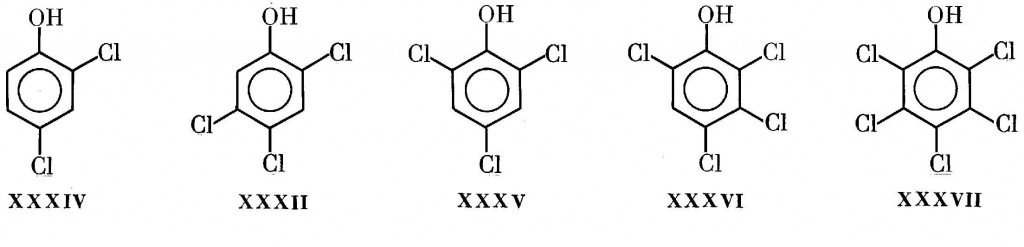
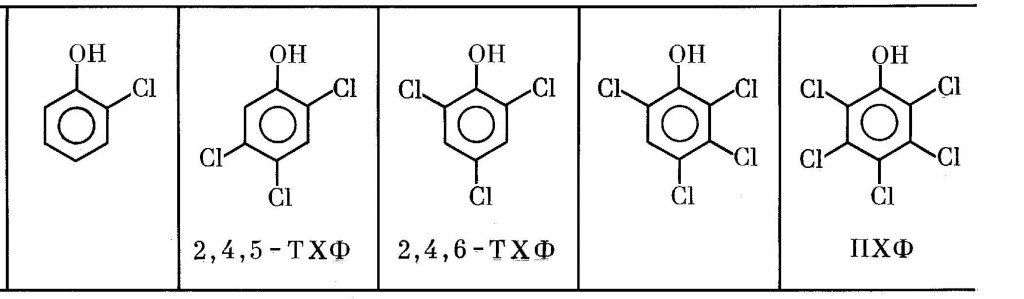
Наиболее мощным источником поступления диоксинов в среду обитания человека долгие годы была да и в настоящее время остается промышленность, занятая производством и переработкой галогенфенолов и галогенанилинов [92,233]. Среди 19 возможных хлорфенолов это относится в основном к 2,4,5- и 2,4,6-ТХФ (XXXII и XXXV), 2,3,4,6-тетрахлорфенолу (XXXVI), ПХФ (XXXVII) и, наконец, 2,4-ДХФ (XXXIV) [3]:
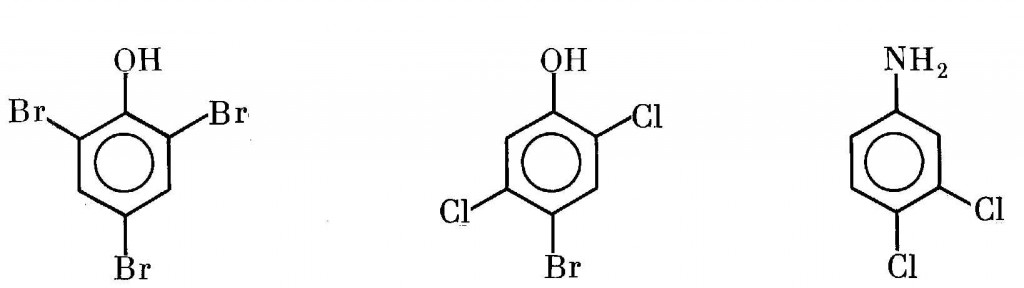
Среди бромфенолов — это 2,4,6-трибромфенол, пентабромфенол и ряд других [53]. Нельзя забывать и о смешанных хлорбромфенолах, например 4-бром-2,5-дихлорфеноле и некоторых других. И, наконец, к тому же ряду веществ относится 3,4-дихлоранилин:
Хлорфенолы широко применяются еще с 30-х годов в качестве различного рода пестицидов (фунгицидов, инсектицидов, антисептиков и т.д.). Они являются также технологическими предшественниками многих других продуктов. В частности, хлорфенолы XXXII и XXXVII — исходные продукты при производстве ряда гербицидов, например, на основании феноксиуксусных кислот — 2,4,5-T, 2,4-Д и др. 2,4,5-ТХФ (дауцид-2) широко применялся при синтезе антибактериального препарата ГХФ XXXVIII [3]. Бромфенолы используются в основном в качестве антипиренов, пестицидов, а также промежуточных продуктов для синтеза ряда соединений.
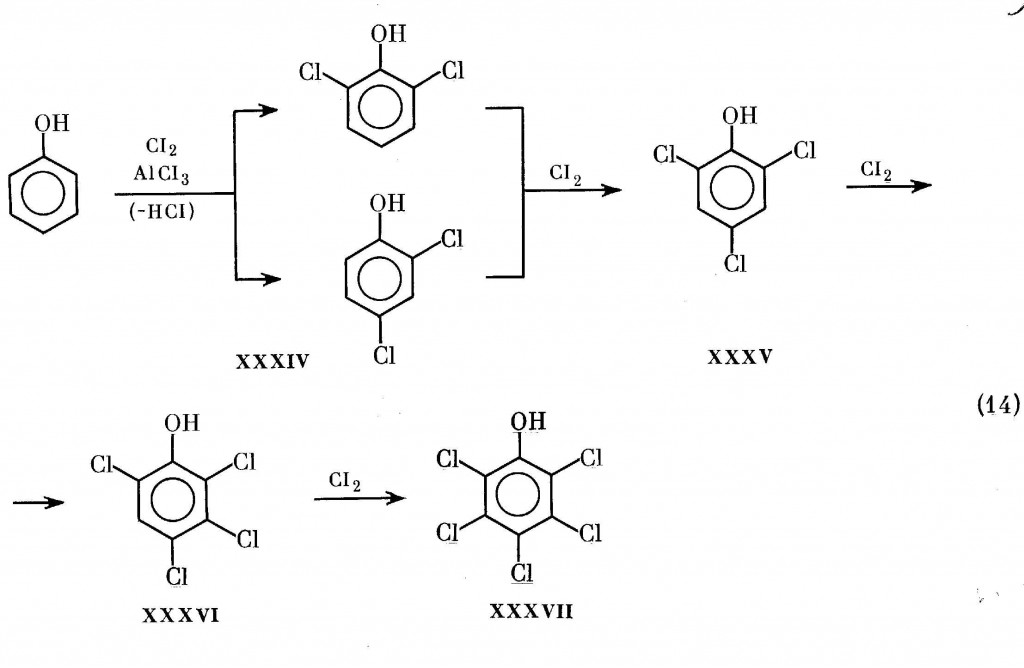
В промышленности хлорфенолы, как правило, получают по реакции (14), т.е. путем прямого каталитического хлорирования фенола:
Глубина прохождения процесса зависит от целей синтеза и избранных условий. Продукты, как правило, очищаются перегонкой.
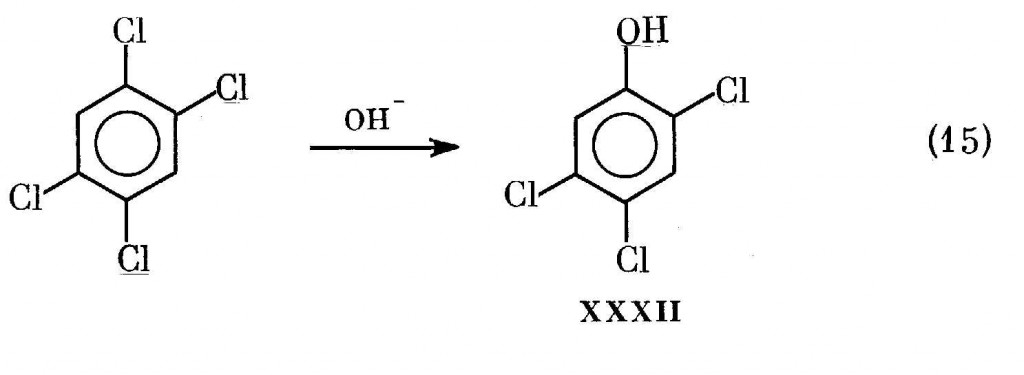
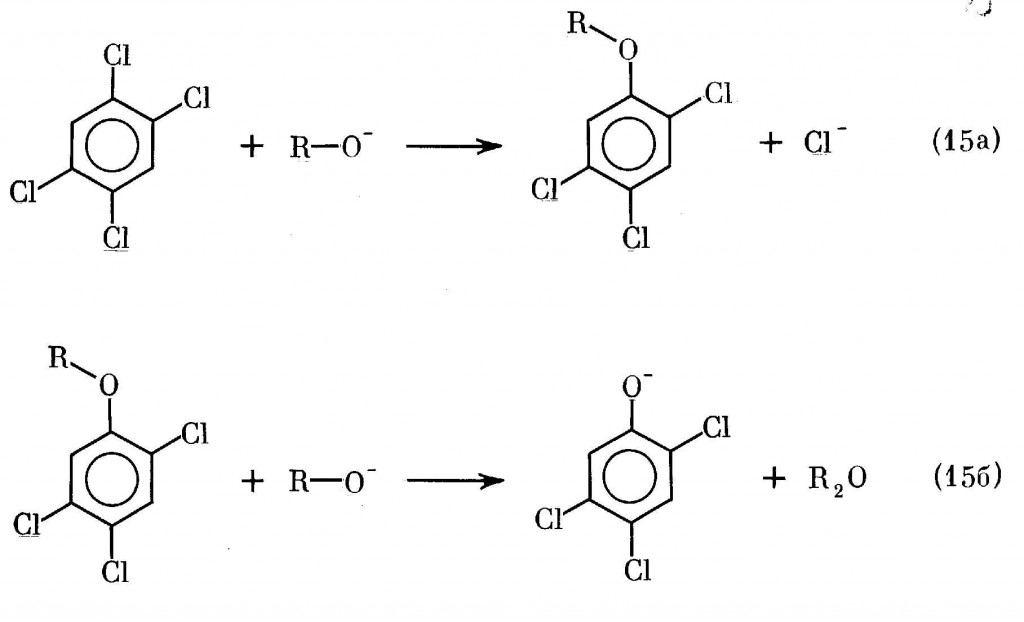
Поскольку в процессе (14) 2,4,5-ТХФ не образуется, его получают путем щелочного гидролиза 1,2,4,5-тетрахлорбензола, синтезируемого из о-дихлорбензола, по реакции (15):
В промышленности щелочной гидролиз 1,2,4,5-тетрахлорбензола по этой реакции осуществляется обычно в спиртовой среде. Исследование кинетики и механизма этой реакции [455,456] показало, что механизм (15) — это не более чем упрощенное изображение процесса. Как уже говорилось в разд.III.2, в действительности она представляет собой последовательный двухступенчатый процесс:
Первоначально при взаимодействии 1,2,4,5-тетрахлорбензола с алкоголятом натрия (15а) образуется соответствующий алкиловый эфир 2,4,5-ТХФ. Его расщепление по реакции (15б) происходит в спиртовых средах с разрывом связи O-R. Обе стадии процесса (15) являются реакциями нуклеофильного замещения и имеют второй кинетический порядок, т.е. протекают по механизму SN2.
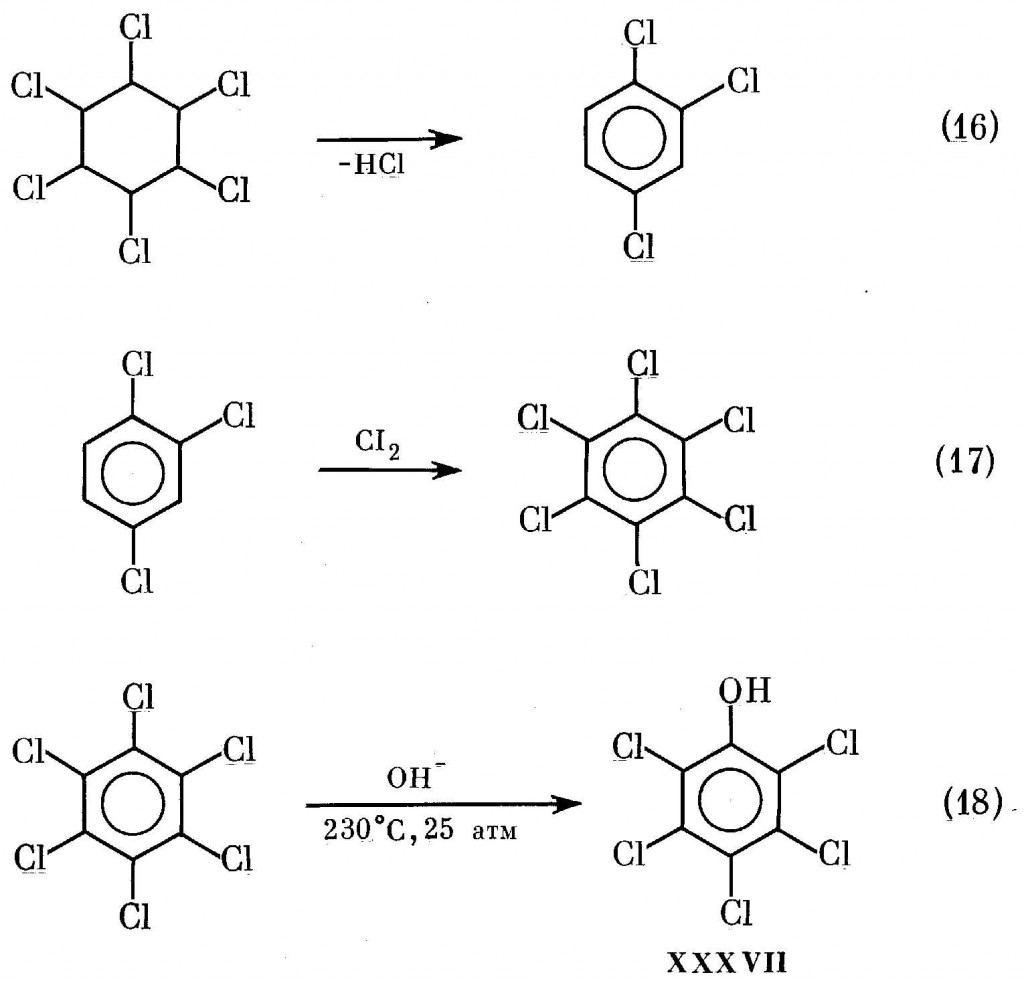
При производстве ПХФ XXXVII обычно используют одну из технологий — (14) [3], а также (16)-(18) [370,377,493]:
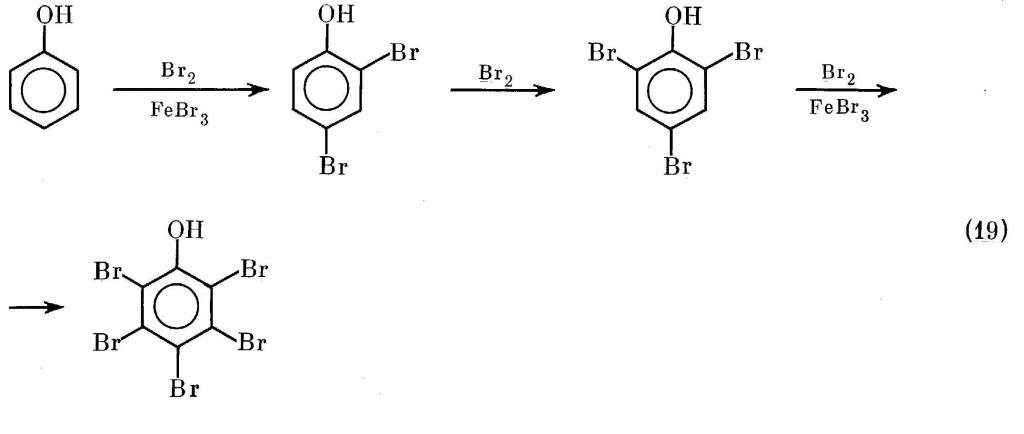
Технологии производства бромфенолов, по существу, аналогичны. Это прямое бромирование фенола (19), в основном каталитическое [3,53]:
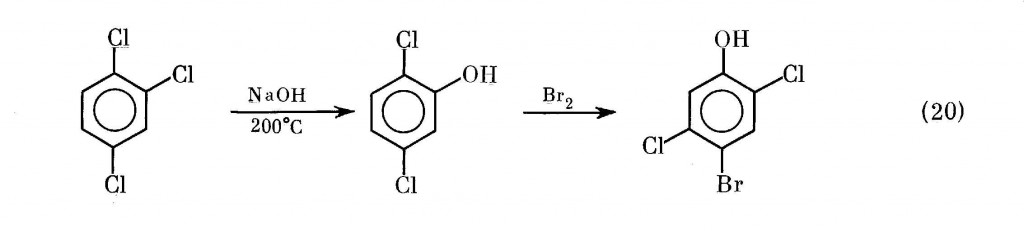
Синтез 4-бром-2,5-дихлорфенола осуществляется по более сложной схеме (20) [53]:
В бывшем СССР в послевоенные годы выпуск хлорфенолов осуществлялся главным образом на предприятиях г.Рубежное (Луганская область), Уфы (Башкирия) и Чапаевска (Самарская область). 2,4,5-ТХФ выпускался с 50-х годов и до 1962 г. на Рубежанском ПО «Краситель», а в 1963-1973 гг. и в 1975-1988 гг. — на Уфимском ПО «Химпром». С 1967 г. на заводе химических удобрений (Чапаевск) действует мощное производство ПХФ XXXVII. Бромфенолы производит УПО «Галоген» (Пермь).
Производство 2,4-ДХФ на ПО «Химпром» (Уфа) по реакции (14) осуществлялось по технологии не каталитического, а высокотемпературного (180°С) хлорирования фенола. Как следствие, процесс сопровождается образованием 2,4,6-ТХФ XXXV, 2,6-ДХФ, а также 2,3,4,6-тетрахлорфенола XXXVI. Разделение хлорированной массы не производилось.
Процесс (15) долгие годы был, по существу, единственным путем к 2,4,5-ТХФ, и все послевоенные годы вплоть до 80-х годов он широко использовался крупнейшими химическими фирмами мира. Этот процесс много лет функционировал на Рубежанском ПО «Краситель», а в 1963-1988 г.г. — на Уфимском ПО «Химпром».
ПХФ по реакции (14) получают обычно в США [3]. В процессе щелочного гидролиза гексахлорбензола (ГХБ)(18), применявшемся в бывшем СССР [494], в качестве исходного сырья обычно использовали малотоксичные изомеры гексахлорциклогексана (ГХЦГ) [370,493,495]. Последние образуются при промышленном выпуске широко употребляемого пестицида линдана (гамма-изомера ГХЦГ) и по реакциям (16) и (17) преобразуются в ГХБ [496].
Процессы (16)-(18) применялись в 1967-1981 гг. на заводе химических удобрений в Чапаевске для выпуска ПХФ, а их заключительная стадия (18), т.е. стадия высокотемпературного гидролиза водной щелочью под давлением, применялась для этих целей до последних лет. В качестве сырья использовалась смесь хлорбензолов (производитель ПО «Химпром», Уфа), дохлорируемая по реакции (17) до ГХБ [377].
С диоксинами, образующимися в процессе производства галогенфенолов, в первую очередь сталкиваются рабочие. Например, в состав технических хлорфенолов, образующихся по реакциям (14), (15) и (18), обычно входят две группы примесей, важных для настоящего обсуждения. Это, во-первых, феноксифенолы (предиоксины) [251,464,465]. Их содержание в хлорфенолах может доходить до 5% [187]. Во-вторых, собственно 2,3,7,8-ТХДД и вообще соединения диоксинового ряда ПХДД и ПХДФ. Суммарная концентрация этих микропримесей составляет обычно 1-2000 и 50-200 ppm соответственно [49,463]. Микропримеси, образующиеся при синтезе бромфенолов, аналогичны.
В табл.4, взятой из работы [53], в качестве примера приводятся данные о содержании примесей диоксинов ПХДД и ПХДФ в некоторых хлорфенолах. Она носит, скорее, справочный характер, поскольку реальное содержание диоксинов в отдельных галогенфенолах может изменяться не только от фирмы к фирме, но и — при неустойчивой технологии — от партии к партии. Однако табл.4 достаточно определенно выявляет тенденции преимущественного возникновения тех или иных видов диоксинов, независимо от условий, складывающихся в том или ином месте или процессе.
Содержание ПХДД и ПХДФ в хлорфенолах (в ppm) [53]
| Соединение | 2-хлорфенол | 2,4,5-ТХФ | 2,4,6-ТХФ | 2,3,4,6-тетра-хлорфенол | ПХФ |
| III (ПХДД) | |||||
| Cl2-ДД | - | 0,72 | - | - | - |
| Cl3-ДД | - | - | 93 | - | - |
| Cl4-ДД | 0,037 | 0,30 | 49 | - | 1,25 |
| Cl5-ДД | - | 1,5 | - | - | 0,08 |
| Cl6-ДД | - | - | - | 4,1-29 | 42 |
| Cl7-ДД | - | - | - | 5,1 | 870 |
| Cl8-ДД | - | - | - | 0,17 | 3660 |
| IV (ПХДФ) | |||||
| Cl3-ДФ | - | - | 1,5 | 0,5 | - |
| Cl4-ДФ | - | - | 2,3-17,5 | 10 | 0.4-0,9 |
| Cl5-ДФ | - | - | 0,7-36 70 | 4-40 | |
| Cl6-ДФ | - | - | 0,02 | 70 | 0,03-90 |
| Cl7-ДФ | - | - | 4,8 | 10 | 0,8-400 |
| Cl8-ДФ | - | - | - | - | 1,3-260 |
Как видно, при производстве три- и тетрахлорфенолов образуются обычно значительные количества диоксинов группы ПХДД (до 1000 ppm). То же относится к ПХФ [497,498]. В частности, в США, крупнейшем производителе ПХФ, выпуск которого осуществляется в основном по реакции (14), конечный продукт содержит в виде примесей от 3 до 7% тетрахлорфенола XXXVI, до 30 ppm различных Cl6-ДД и смесь различных ПХДФ IV. Наиболее токсичный диоксин I не всегда находят в значительных количествах, однако в 2,4,6-ТХФ, например, где его в принципе не должно быть, его концентрация оказалась достаточно большой — 0,5 ppm [54].
О наличии диоксинов в бромфенолах известно меньше, однако ПБДД (V) и ПБДФ (VI), главным образом ТБДД и ТБДФ, уже обнаружены и определены в техническом 2,4,6-трибромфеноле [297].
В процессе выпуска 2,4-ДХФ, производимом по реакции (14), но осуществляющемся по высокотемпературной технологии, образование значительных количеств ПХДД и ПХДФ неизбежно. Это связано с тем, что даже при строгом выдерживании технологического регламента содержание продуктов перехлорирования велико, и оно резко возрастает при технологических нарушениях. Схема 4 демонстрирует некоторые пути образования только лишь ПХДД, принципиально возможных при само- и взаимоконденсации фенолов в тех реальных условиях, которые складываются, например, на ПО «Химпром» (Уфа).
Выполненный в 1990 г. анализ технического 2,4-ДХФ, используемого на ПО «Химпром» (Уфа) при синтезе аминной соли 2,4-Д, подтверждает эти предположения. В сыром продукте были обнаружены многочисленные изомеры и гомологи ПХДД III в концентрации от 0,04 до 0,1 ppb. Кроме того, был найден ряд изомеров ПХДФ IV (измерения НПО «Тайфун», в ppb):
1,3,6,8-ТХДФ — 280
1,2,3,6,8-ПХДФ — 236
неидентифицированный изомер ТХДФ — 147
неидентифицированный изомер ПХДФ — 188
другие ТХДФ, ПХДФ и ГкХДФ — 2,9-6,6
Другая серия измерений, выполненных в октябре 1990 г., свидетельствует о чрезвычайно высокой загрязненности продукции завода, связанной с производством 2,4-Д. В частности, концентрации наиболее токсичных 2,3,7,8-ТХДД и 2,3,7,8-ТХДФ были следующие (в ppb):
| 2,3,7,8-ТХДД | 2,3,7,8-ТХДФ | |
| 2,4-Д, аминная соль | 0,63 | 8,5 |
| 2,4-ДХФ | 0,32 | 43,0 |
В США, где хлорирование по реакции (14) осуществляется в каталитических условиях, загрязнение 2,4-ДХФ и гербицида 2,4-Д диоксинами III и IV обычно незначительно [497]. Однако оно возможно в случае, если производство этих продуктов осуществляется на оборудовании, ранее использовавшемся для производства 2,4,5-ТХФ и гербицида 2,4,5-Т. В частности, в США зарегистрирован случай, когда в кубовых остатках производства 2,4-Д, налаженного на оборудовании, ранее использовавшемся для выпуска 2,4,5-Т, диоксин I в концентрации 70 ppb был найден через 7 лет после прекращения выпуска 2,4,5-Т [49]. То же самое было и на ПО «Химпром» (Уфа) после 1967 г., когда гербицид 2,4-Д несколько лет выпускался на оборудовании, ранее применявшемся для производства 2,4,5-Т. А обнажиться эта проблема могла неоднократно, например осенью 1987 г.,когда в этом цехе произошел пожар. Однако анализы на диоксины после пожара не выполнялись.
При очистке технических хлорфенолов микропримеси диоксинов в значительной степени переходят в отходы производства (разд.IV.3). В частности, диоксины, которые были обнаружены в гербициде 2,4-Д (ПО «Химпром», Уфа), найдены также и в сбросах завода (разд.IV.2.6). Происхождение этих примесей легко видеть из анализа действующих технологий завода.
В ПО «Химпром» (Уфа) в цехах N 2 и N 11 действуют две технологии получения гербицида 2,4-Д — фильтрационная и экстракционная (ТУ 113-04-118-84) [492].
При фильтрационном способе конденсацию натриевой соли 2,4-ДХФ с монохлоруксусной кислотой осуществляют в течение 2-3 ч в щелочных условиях (рН 8,5-9,5) при 100-110°С, поддерживаемой паром. Эти условия благоприятны для образования упоминавшейся смеси реально найденных ПХДД и ПХДФ. После охлаждения суспензия натриевой соли 2,4-Д фильтруется на барабанных вакуумных фильтрах. Фильтрат собирается в емкость и очищается.
При экстракционном способе конденсация происходит в еще более жестких и вновь щелочных условиях. Ее температура поддерживается в интервале 130-160°С с подачей пара 2-3 атм, а объемное соотношение реагентов устанавливается вручную. Конденсированная масса с рН 7-9 попадает в выделитель, куда подаются также HCl, а в качестве экстрагента тетрахлорэтилен.
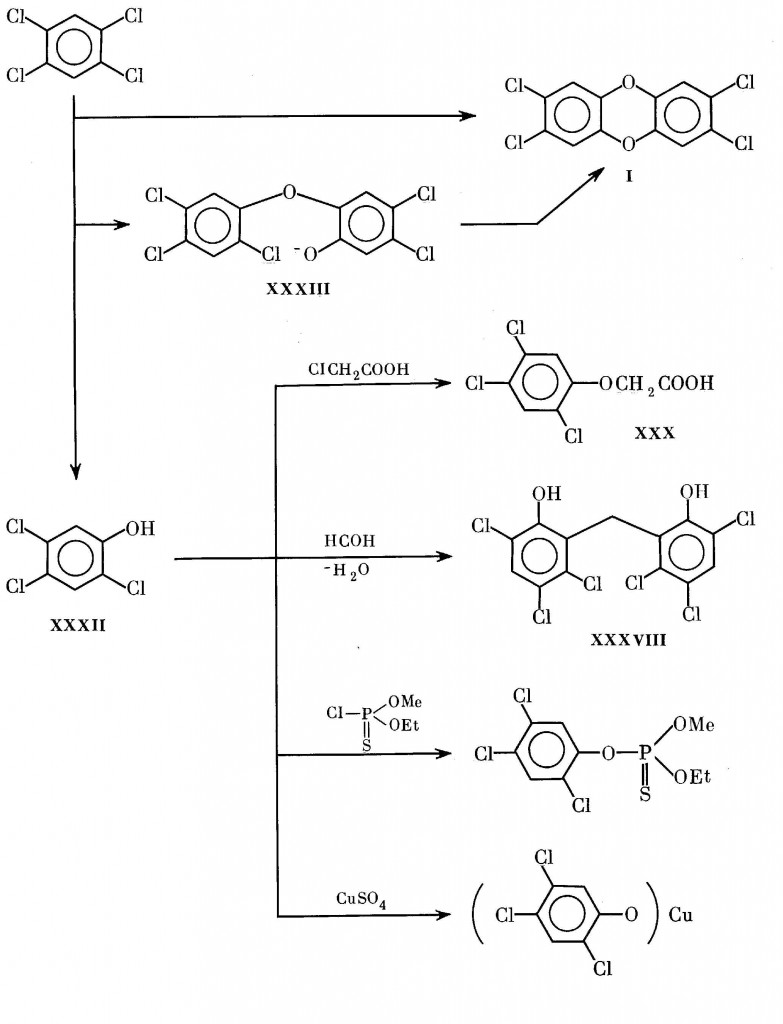
Схема 5. Схема промышленного производства ряда продуктов, осуществлявшегося на основе 1,2,4,5-тетрахлорбензола и 2,4,5-ТХФ
Образование ПХДД и ПХДФ в процессе экстракции будет рассмотрено в разд.IV.2.2. Здесь же следует упомянуть о судьбе сточных вод, образующихся в рамках обеих технологий. По действующим регламентам, они подщелачиваются, после чего обрабатываются хлором в бронированных фторопластом титановых колоннах, заполненных кольцами Рашига. Предполагается, что обработка сточных вод хлором обеспечивает их обесфеноливание с образованием хлормалеиновой кислоты. Однако одновременно происходит резкое увеличение концентрации ПХДД и ПХДФ (см. разд.IV.2.6). Жидкость на выходе из колонн имеет рН 6-7 и после отстоя, при котором концентрация хлорфенолов снижается до < 30 мг/л, сбрасывается в химически загрязненную канализацию.
Отходы, остающиеся после перегонки ПХФ, могут содержать до 2000 ppm ПХДД и ПХДФ [49]. Таким образом, только в 1972-1977 гг. в США фактически было «произведено» несколько тонн этих диоксинов, включая наиболее токсичные [233].
Переработка хлорфенолов в новые продукты сопровождается переходом в последние и диоксиновых микропримесей. Однако их содержание может и резко возрасти за счет предиоксинов, чему, как правило, способствуют условия реакции [243,440].
Особенно большие количества самого токсичного диоксина I, а также других диоксинов образуются при производстве и переработке 2,4,5-ТХФ. Определенное представление об этом дает схема 5. На ней изображены пути образования собственно 2,4,5-ТХФ, а также его превращения в некоторые целевые продукты, получавшиеся и использовавшиеся в бывшем СССР.
2,4,5-ТХФ, производившийся в Уфе на ПО «Химпром», в 1965-1967 гг. перерабатывался в гербицид 2,4,5-Т (бутиловый эфир) непосредственно на месте. Трихлорфенолят меди также выпускался на месте с 1975 г. по 1987 г., когда производство 2,4,5-ТХФ было прекращено, однако перерабатывался в комбинированный смесевой протравитель семян фентиурам на Первомайском ПО «Химпром» (Харьковская область). 2,4,5-ТХФ поставлялся на другие заводы для последующей переработки в новые продукты — в антибактериальный препарат ГХФ (производитель — Рубежанское ПО «Краситель») и пестицид трихлорметафос-3, а также смесевой препарат трихлороль 5 (производитель — опытный завод ВНИИ химических средств защиты растений в г. Щелково, Московская область).
Само возникновение диоксинов и в особенности их количество непосредственно определяются технологическими условиями. В частности, при производстве 2,4,5-ТХФ это происходит на стадии гидролиза (омыления) 1,2,4,5-тетрахлорбензола, осуществляемого по реакции (15) с помощью NaOH в каком-либо растворителе. Несмотря на обширную патентную литературу [3], в реально осуществленных в индустрии процессах это выполняется обычно в рамках одной из двух технологий — метанольной или этиленгликолевой (последняя считается экономически более выгодной [107]). Соответственно используются реакторы двух типов — автоклавы, в которых процесс ведется в среде метанола под давлением (процесс фирмы «Берингер», ФРГ), или же обычные реакторы, в которых реакция проводится при нормальном давлении в среде этиленгликоля (процесс фирмы «Доу Кемикал», США, запатентованный еще в 1950 г.). Для течения реакции (15) и «диоксиновой чистоты» получаемого 2,4,5-ТХФ важны выбор и соблюдение условий процесса.
Исторический опыт, сопровождавшийся рядом массовых поражений работников (см. разд.IV.1.7), позволил найти условия, обеспечивающие по возможности минимальную концентрацию 2,3,7,8-ТХДД в сыром, еще неперегнанном 2,4,5-ТХФ:
| Технология | Растворитель Т,oС | Давление,атм |
| «Берингер» | Метанол | 157 19,5 |
| «Доу Кемикал» | Этиленгликоль | 160-180 (См.*) - |
| * Условия стандартной технологии, когда поражений персонала не наблюдалось. Фактически на фирме «Доу Кемикал» в 1964 г. в период форсированного выпуска 2,4,5-Т, стимулированного войной во Вьетнаме, использовалась температура выше 200°С [107]. | ||
Оптимальные условия гидролиза ГХБ — температура от 125 до 175°С, растворитель — метанол. Эти условия были реализованы при получении коммерческого продукта в США [3].
Как будет показано в разд.IV.1.7, фирмы, не знавшие (до 1957 г.) или же не учитывавшие опасности образования больших количеств 2,3,7,8-ТХДД, не выдерживали экологически оптимальных условий процесса (15). Это приводило к поражениям работников, сбоям в работе оборудования, срывам поставок.
В частности, стремление производителей ускорить щелочной гидролиз 1,2,4,5-тетрахлорбензола, несмотря на отработанность минимально опасной метанольной технологии, нашло закрепление в патентной литературе. В США, например, были запатентованы две технологии, предполагавшие гидролиз (15) при более высоких температурах: метанольную с поднятием температуры процесса до 220°С (1967 г.) и водяную с рабочим диапазоном температур от 225 до 300°С (1957 г.) [3]. В бывшем СССР был оформлен аналогичный документ, в котором был предложен способ синтеза, «отличающийся тем, что для ускорения процесса и повышения выхода целевого продукта омыление проводят при 200-230°С» [499].
Обосновывалось это стремление и теоретически [456,500]. В 1961 г. в бывшем СССР, в частности, было опубликовано сообщение о необходимости ведения процесса (15) при 220-230°С и соответственно более высоком давлении [457,499]. Новшество обещало завершение реакции за 0,5 ч вместо 14-16 ч и было реализовано на пилотной установке Рубежанского ПО «Краситель», а в 1965 г. — в специально построенном цехе N 19 Уфимского ПО «Химпром». В предложенной и фактически реализованной форме эта идея совершенно не учитывала образования — вместе с ростом выхода целевого продукта — больших количеств высокотоксичного 2,3,7,8-ТХДД [280-285]. Ее осуществление привело к массовому профессиональному поражению работников завода [92,376,501-504].
Недавно было вновь упомянуто о возможности проведения гидролиза (15) при повышенных температурах [505]. Речь идет об идее получения 2,4,5-ТХФ по непрерывной схеме, хотя автор и сознает опасность загрязнения целевого продукта диоксином I.
Гидролиз ГХБ водной щелочью по (18), реализованный на Чапаевском заводе химических удобрений, также предусматривает жесткие условия — температуру выше 230°С и давление выше 25 атм [506]. Они были заложены в процесс с самого начала [493, 495] и, несмотря на поражения работников производства ПХФ [507,508], остались неизменными до наших дней [370].
В принципе при производстве 2,4,5-ТХФ, не сопровождающемся нарушениями экологически оптимального температурного режима, содержание в нем 2,3,7,8-ТХДД уже может достигать в зависимости от особенностей применяемой технологии, условий реакции и других обстоятельств, недопустимо больших величин (6,2 ppm [497], 10-25 ppm [311], 27,8 ppm [509] и больше). Однако при температурах от 220 до 300°С, предусмотренных некоторыми патентами, содержание 2,3,7,8-ТХДД может возрасти и до 1600 ppm (растворитель — метанол или вода) [33,49].
В связи с этими обстоятельствами в 60-х годах, наряду с экологической оптимизацией технологии получения, были ужесточены требования к очистке продукта. Технологии западных стран предусматривали предварительную обработку реакционной массы (после окончания реакции (15), удаления растворителя и заполнения реактора водой). Имеется в виду промывка натриевой соли 2,4,5-ТХФ толуолом для удаления наиболее высоколетучих органических примесей типа диоксина [3]. Кроме того, в технологию вводились заключительные стадии перегонки 2,4,5-ТХФ [3,348].
В Великобритании уже в начале выпуска 2,4,5-ТХФ, осуществленного в 1965 г., технология содержала обязательные стадии перегонки сырого продукта (т.пл. ТХФ 65-65,5°С для чистого продукта и 60-63°С — для неочищенного). 2,4,5-ТХФ, предназначавшийся для дальнейшего превращения в продукты сельскохозяйственного назначения, например в гербицид 2,4,5-Т, подвергался однократной перегонке, а направлявшийся для использования в фармацевтических целях (например, для преобразования в антибактериальный препарат ГХФ) — двукратной [348]. Поставка потребителям неперегнанного 2,4,5-ТХФ исключалась.
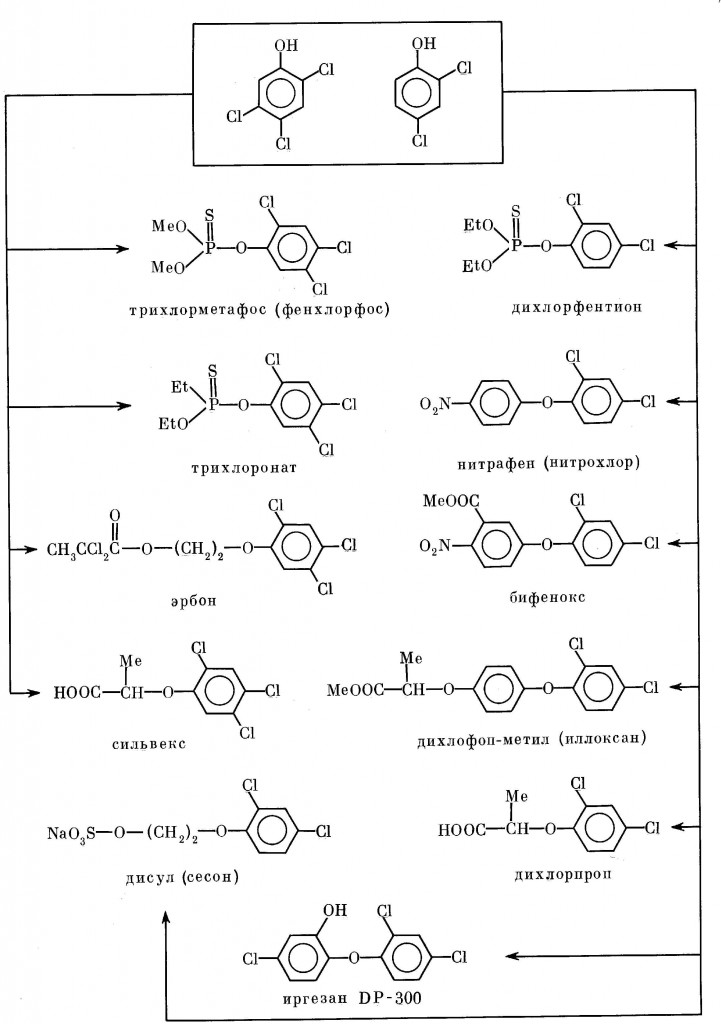
Схема 6. Некоторые широкоупотребительные пестициды, получаемые на основе 2,4,5-ТХФ и 2,4-ДХФ
В бывшем СССР 2,4,5-ТХФ, выпускавшийся до 1988 г. в уфимском ПО «Химпром» для первых и вторых целей, не подвергался ни толуольной очистке, ни перегонкам и отправлялся непосредственно потребителям. Содержание 2,3,7,8-ТХДД на момент прекращения выпуска составляло в зависимости от партии от 0,99 до 30 ppm.
Как уже говорилось, в конечных продуктах содержание токсичного 2,3,7,8-ТХДД может совпадать с таковым в исходном 2,4,5-ТХФ. В ряде случаев оно может существенно возрастать. Это связано с тем, что на завершающих стадиях превращения ТХФ в продукты сельскохозяйственного и фармацевтического назначения происходит превращение содержащегося в них предиоксина XXXIII в собственно 2,3,7,8-ТХДД [82,251]. ГХФ получают реакцией 2,4,5-ТХФ с формальдегидом в кислой среде (при 5, 50-100 или 135°С, в зависимости от процедуры) [53], и эти условия благоприятны для превращения предиоксина в 2,3,7,8-ТХДД.
В 60-х годах не было необычным содержание в гербициде 2,4,5-Т наиболее токсичного 2,3,7,8-ТХДД 30-40 ppm [87,335]. Вообще же в гербицидах 2,4,5-Т и сильвексе эта величина могла доходить в этот период до 70 ppm [82] и даже до 100 ppm [510].
Введение в технологию выпуска 2,4,5-ТХФ стадий промывки толуолом и перегонки позволило резко улучшить положение, поскольку при этом удавалось освободиться от значительной части не только диоксина, но также и предиоксинов. Так, например, после 1971 г. многие производители США снизили содержание диоксина I до 1 ppm [87]. В дальнейшем в связи с ужесточением нормативов оно было снижено до 0,1 ppm (1972-1974 гг., Швеция [510]; 1979 г., США [87]), а затем и до 0,01 ppm [66].
В бывшем СССР вопрос о содержании 2,3,7,8-ТХДД в гербициде 2,4,5-Т никогда не ставился, и соответствующие измерения не производились. Первые определения концентрации 2,3,7,8-ТХДД в 2,4,5-ТХФ были выполнены лишь в 1987-1988 гг. в момент закрытия этих производств. Достоянием общественности и объектом публичного обсуждения они не стали. Определение диоксина I в отечественном ГХФ, выпускавшемся на Рубежанском ПО «Краситель» из уфимского 2,4,5-ТХФ, было проведено в 1987-1988 гг., и его содержание доходило в это время до 102 ppm. После этого выпуск ГХФ был прекращен (разд.IV.2.8).
Наличие диоксинов в многочисленных пестицидах, выпускаемых на основе моно-, ди- и трихлорфенолов, не обсуждалось столь широко, как в случае 2,4,5-Т. Речь идет о таких продуктах, как дихлорпроп, дихлофентион, дикамба (банвел 9), нитрофен (нитрохлор), бифенокс, фенхлорфос (роннел), эрбон, трихлоронат и многие другие [3,53]. Часть из них приведена на схеме 6. Все эти соединения не могут не нести в себе значительных количеств 2,3,7,8-ТХДД и других ПХДД и ПХДФ, образовавшихся в момент синтеза. Более подробно этот вопрос будет рассмотрен в разд.IV.2.7, а здесь ограничимся лишь несколькими примерами, относящимися к бромсодержащим фенолам и хлоранилинам.
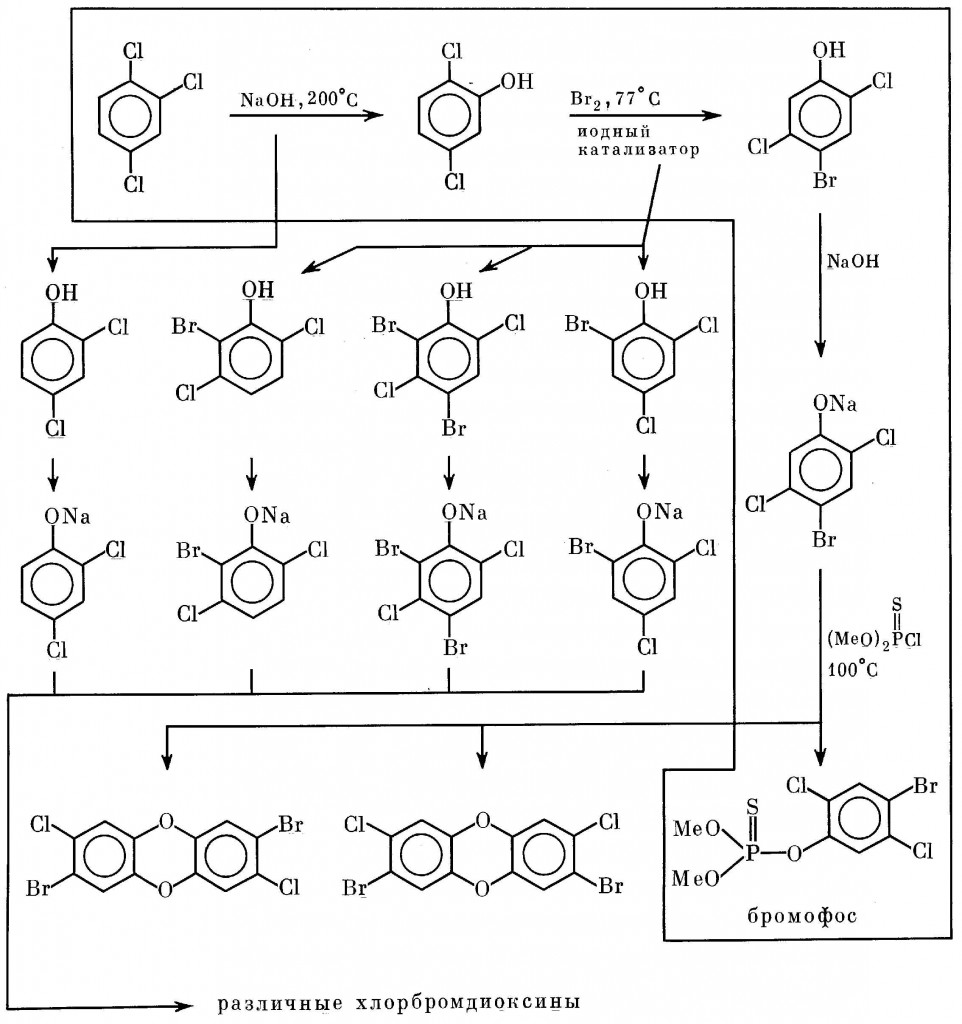
Схема 7 демонстрирует последовательность реакций, ведущих к образованию бромофоса, введенного в широкую практику в 1964 г. Этот инсектицид, обладающий низкой токсичностью по отношению к теплокровным, был разработан фирмой «Берингер» [53]. Схема демонстрирует также канонические пути попутного возникновения диоксинов, опасных для персонала соответствующих цехов.
Схема 7. Промышленное производство бромофоса (выделен основной процесс, вне его — побочные реакции)
В действительности дело обстоит много сложнее. Измерения, выполненные на примере одной из промышленных партий бромофоса, показали [53], что конечный, уже очищенный продукт может также содержать довольно значительные количества высокохлорированных ПХДД и ПХДФ (в ppb):
ГкХДД — 25 ГкХДФ - 10
ГпХДД — 400 ГпХДФ - 30
ОХДД - 800 ОХДФ — 45
Примеси бромированных диоксинов, возможно, оказались вне процесса анализа, хотя их появления в смеси можно было ожидать по крайней мере в неменьших количествах.
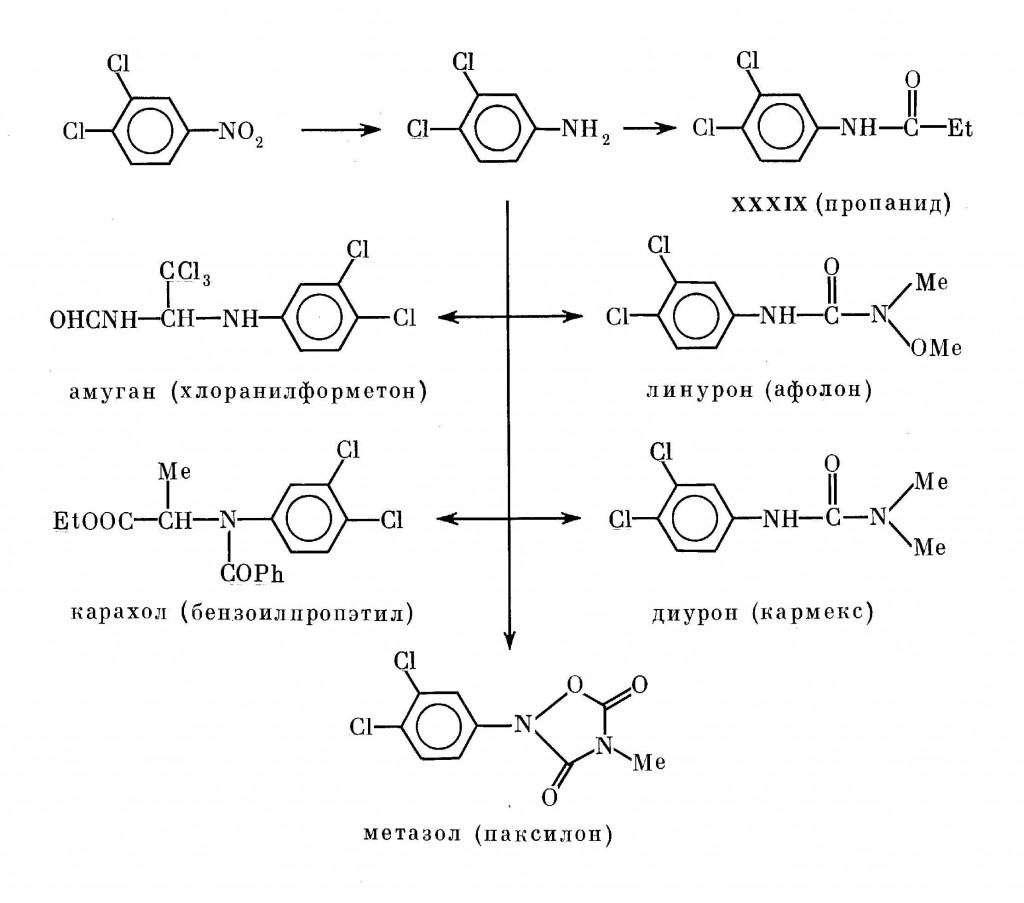
Другой пример касается серии пестицидов, полученных на основе 3,4-дихлоранилина, и в первую очередь пропанида XXXIX — гербицида, широко применяемого в нашем рисоводстве. Производство пропанида базируется на гидрировании 3,4-дихлорнитробензола в толуоле под давлением примерно 200 атм [370,511].
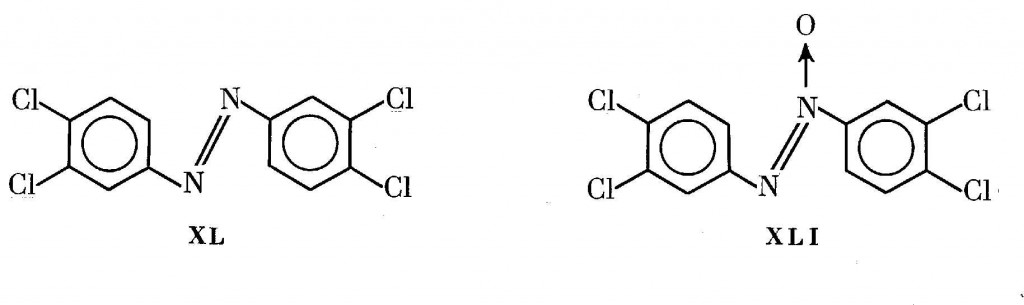
В принципе, как видно из многообразия пестицидов, приведенного на схеме и включающего лишь наиболее широко употребляемые пестициды из числа созданных, этот процесс вполне мог рассматриваться как перспективный. Он был разработан в Уфе [512] и внедрен в ПО «Синтез» (Дзержинск). Однако безопасность по диоксину для работников завода не только не предусматривалась разработчиками, но даже не рассматривалась ими. Были проигнорированы также известные данные [171,172,308,513,514] об образовании при производстве пропанида и других гербицидов этого ряда хлоракнегенных примесей типа XIII и XIV, а именно 3,4,3′,4′-тетрахлоразобензола XL и продукта его окисления 3,4,3′,4′-тетрахлоразоксибензола XLI:
Даже для новых производственных мощностей, вводившихся совсем недавно, в 1988-1989 гг., содержание микропримеси диоксинов и родственных соединений регламентировано не было.
Гигиеническое обследование работников завода, выполненное в 70-х годах, показало, что фактически созданное крупномасштабное производство пропанида оказалось чрезвычайно несовершенным. Было выявлено, в частности, что влияние вредных факторов на здоровье работающих проявляется в виде угрей у части рабочих, занятых как на основных производственных стадиях, так и на стадии уничтожения его отходов. Найдены также поражения внутренних органов [515].
Как выяснилось много позже [511], cерьезных усовершенствований в процесс так и не было внесено. Пробный анализ одного из образцов отечественного пропанида, выполненный еще позже, в 1987 г., показал наличие в нем только лишь 2,3,7,8-ТХДД в концентрации 6,0 ppb. В сточных водах этого производства концентрация 2,3,7,8-ТХДД доходила до 3,7 ppb. Другие анализы не производились, равно как и не определялись другие соединения классов ПХДД и ПХДФ. Учитывая, что, по условиям этой технологии, возникновение примеси 2,3,7,8-ТХДД вероятно в наименьшей степени, можно лишь догадываться о примесях полихлорированных азо- и азоксибензолов XL и XLI, содержание которых должно было быть особенно значительным и анализы на которые не выполнялись.
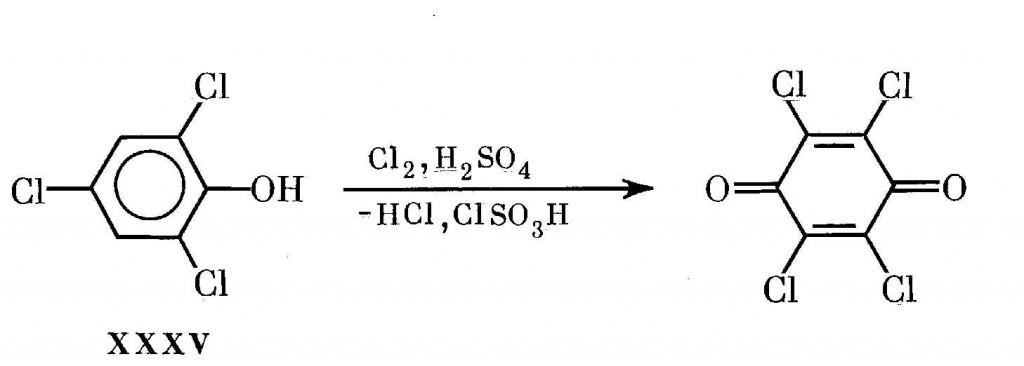
Важным продуктом химической промышленности является хлоранил (2,3,5,6-тетрахлор-1,4-бензохинон). В практике это соединение используют в качестве активного наполнителя при изготовлении особо прочных автомобильных тормозных колодок. Его применяют также как промежуточный продукт при производстве диоксазиновых красителей, например ярко-голубого светопрочного, при изготовлении специальных каучуков или же непосредственно в качестве фунгицидов при протравливании бобовых и хлопчатника [370,492,493,516]. Получают хлоранил из 2,4,6-ТХФ путем его хлорирования не по реакции (14), а избытком газообразного хлора в течение 10-12 ч при 100-110°С в сильнокислой среде [370,490,493,516]:
По способу получения хлоранил неизбежно должен содержать примеси ПХДД, образующиеся вместе с 2,4,6-ТХФ, а также вновь генерируемые в процессе синтеза собственно хлоранила. Эти микропримеси действительно были найдены во всех исследованных зарубежных коммерческих образцах хлоранила (ОХДД — на уровне ppm, а ГпХДД и ПнХДД — на уровне ppb) [517-519]. Предварительные данные показывают, что при переработке хлоранила в пигмент концентрации ПХДД и ПХДФ не возрастают [518].
Вопрос о примесях диоксинов в хлораниле, производящемся в объеме 300 т в год в цехе N 16 в ПО «Химпром» (Уфа), никогда не ставился. Не рассматривается он и в справочных документах [370,493]. Все жидкие и газообразные отходы этого производства сбрасываются в канализацию [516]. Усовершенствованный процесс выпуска хлоранила, разработанный в ГосНИИхлорпроекте, также не предусматривает каких-либо специальных мер по предотвращению образования диоксинов [516].
Первые же измерения, выполненные в последние годы, показали, что это производство действительно опасно. Как оказалось, в пробах 2,4,6-ТХФ, отобранных в октябре 1990 г., только высокoтоксичные изомеры ПХДД и ПХДФ содержались в чрезвычайно высоких концентрациях (в ppb):
2,3,7,8-ТХДД — 1,1
1,2,3,7,8,9-ГкХДД - 0,85
1,2,3,4,6,7,8-ГпХДД - 546,0
ОХДД - 12,6
2,3,7,8-ТХДФ — 43,0
Зимой 1991-1992 г.г. производство было прекращено.
| « Назад | Оглавление | Вперед » |