ДИОКСИНЫ И ЖИВЫЕ ОРГАНИЗМЫ
V.2. Токсичность
Биологическая активность диоксинов обычно выражается концентрацией субстрата, вызывающей 50%-ное повышение активности цитохрома Р-448 от максимально возможного. Разработан ряд других способов оценки токсических свойств диоксинов — по индукции бензпирен-гидроксилазы (7-этоксирезоруфин-О-деэтилазы) в микросомах печени, по потере веса тела (увеличению отношения веса печени и всего тела), по степени атрофии тимуса [139].По-видимому, первые сообщения об острой токсичности именно диоксина, в частности 2,3,7,8-Hal4-ДД, относятся к 1957 г. Люди, осуществлявшие синтез 2,3,7,8-ТХДД [281] и 2,3,7,8-ТБДД [285], получили поражение и были госпитализированы [248,282]. Позднее сообщалось и о других случаях острого поражения исследователей от диоксина I [808].
После получения первых данных о высокой острой токсичности некоторых диоксинов III и IV [140,142,145,147] и их бромсодержащих аналогов V и VI [141,787] появились многочисленные работы, посвященные систематическому изучению токсикологических особенностей веществ [138,140-149,158,160,161], в том числе их острой, подострой и хронической токсичности.
Данные об острой токсичности диоксинов получены на животных. Хроническое действие исследовано как на животных, так и на людях, оказавшихся пораженными по тем или иным причинам — при авариях, при прямом контакте с гербицидами на сельскохозяйственных работах или же в период военных действий и т.д. Известны и специальные опыты на добровольцах [144,778].
V.2.1. Острая токсичность
Сведения об острой токсичности диоксинов и ряда других высокотоксичных веществ приведены в табл.11 и 12, составленных по результатам [56,142,147,151,788,809-811], относящимся к подопытным животным. Как видно, токсичность диоксинов существенно зависит от видовых особенностей подопытных животных, что связывают с различиями в скорости его выведения из организма [812].
Среднесмертельная доза для человека, полученная расчетным путем, составляет при однократном оральном поступлении 0,05-0,07 ppm [813].
Острая токсичность некоторых диоксинов III-VI [57,147,788]
| Соединение | LD5, мкг/кг | |||
| морская свинка | обезьяна | мышь | крыса | |
| III (ПХДД) | ||||
| 2,3-Cl2-ДД | - | - | - | >1000000 |
| 2,7-Cl2-ДД | - | - | >2000000 | >1000000 |
| 2,8-Cl2-ДД | >300000 | - | 874000 | >5000000 |
| 1,3,7-Cl3-ДД | - | - | >15000000 | >5000000 |
| 2,3,7-Cl3-ДД | 29444 | - | >3000 | >1000000 |
| 1,2,3,4-Cl4-ДД | - | - | - | 1000000 |
| 1,3,6,8-Cl4-ДД | >15000000 | - | >2987000 | >1000000 |
| 2,3,7,8-Cl4-ДД | 0,6-2,0 | 70 | 114-284 | 22-45 |
| 1,2,3,7,8-Cl5-ДД | 3,1 | - | 337,5 | - |
| 1,2,4,7,8-Cl5-ДД | 1125 | - | >5000 | - |
| 1,2,3,4,7,8-Cl6-ДД | 72,5 | - | 825 | - |
| 1,2,3,7,8,9-Cl6-ДД | 60-100 | - | >1440 | - |
| 1,2,3,6,7,8-Cl6-ДД | 70-100 | - | 1250 | - |
| 1,2,3,4,6,7,8-Cl7-ДД | >600 | - | - | - |
| Cl8-ДД | - | - | >4000000 | >1000000 |
| IV (ПХДФ) | ||||
| 2,8-Cl2-ДФ | - | - | >15000000 | >15000000 |
| 2,4,8-Cl3-ДФ | - | - | >15000000 | >5000000 |
| 2,3,7,8-Cl4-ДФ | 5-10 | 1000 | >6000 | >1000 |
| 2,3,4,7,8-Cl5-ДФ | 3-10 | - | - | 916 |
| 2,3,4,6,7,8-Cl6-ДФ | 120 | - | - | - |
| V (ПБДД) | ||||
| 2,3,7,8-Br4-ДД | - | - | - | <1000 |
| VI (ПБДФ) | ||||
| 2,3,7,8-Br4-ДФ | <15 | - | - | - |
Как следует из табл.11, максимальной токсичностью обладает собственно 2,3,7,8-ТХДД I [142], хотя известны также и несколько более токсичные [357]. Помимо диоксина I, чрезвычайно высокой токсичностью обладает 1,2,3,7,8-Cl5-ДД. Близки по токсичности также некоторые хлорированные производные фуранового ряда ПХДФ (в особенности родоначальник ряда 2,3,7,8-ТХДФ II и два Cl5-изомера — 1,2,3,7,8- и 2,3,4,7,8-Cl5-ДФ) [810]. Токсичность указанных диоксинов на много порядков выше таковой ДДТ, а также токсичности цианидов, стрихнина, кураре [814,815]. Столь же высока токсичность некоторых броморганических производных ПБДД и ПБДФ, в первую очередь броморганических аналогов I и II, а также 2,3,7-Br3 [141,787]. Высока токсичность cоответствующих смешанных хлорброморганических соединений VII и VIII [301]. В целом соединения семейств ПХДД и ПХДФ менее токсичны, чем родоначальники этих рядов I и II, хотя не все представители семейств III и IV, а тем более V-VIII, изучены в токсикологическом плане столь же подробно [147].
Острая токсичность некоторых наиболее токсичных
| Соединение | LD5, мкг/кг | ||
| морская свинка | обезьяна | мышь | |
| ПХДД с дополнительным негалогенидным заместителем | |||
| 1-NO2-2,3,7,8-Cl4-ДД | 47,5 | - | >2000 |
| 1-NH2-2,3,7,8-Cl4-ДД | 194,2 | - | >4800 |
| 1-NO2-3,7,8-Cl3-ДД | >30000 | - | - |
| 1-NH2-3,7,8-Cl3-ДД | >30000 | - | - |
| Полибромбифенилены | |||
| 2,3,6,7-Br4-бифенилен | >10 | - | - |
| Полигалогеннафталины | |||
| 2,3,6,7-Cl4-нафталин | >>3000 | - | - |
| 2,3,6,7-Br4-нафталин | 206 | - | - |
| . | 200 | - | - |
| . | 361 | - | - |
| ПХБ | |||
| 3,4,3′,4′-Cl4-бифенил | <1000 | - | - |
| 3,4,5,3′,4′,5′-Cl6-бифенил | 500 | - | - |
| 2,3,4,5,3′,4′,5′-Cl7-бифенил | >3000 | - | - |
| Хлорорганические инсектициды | |||
| ДДТ | - | - | 200000 |
| Антихолинэстеразные ОВ | |||
| Табун | - | 208 | - |
| Зарин | 38 | 83 | 100 |
| Зоман | - | 156 | - |
| VX | 8,4 | 20,1 | 50 |
В табл.12 собраны данные по токсичности диоксиноподобных веществ более широкого круга, а также высокотоксичных веществ иной природы. Из этой таблицы следует, что высокой токсичностью обладают также некоторые галогенидные производные нафталина и бифенилена [151]. Более того, значительна токсичность нескольких ПХБ из числа тех, что не имеют атомов галогена в орто-положении ко второму кольцу (в класcификации IUPAC: ПХБ N 77, 126 и 169) [151]. Наконец, к числу высокотоксичных диоксинов относятся также 3,4,3′,4′-тетрахлоразобензол XL и 3,4,3′,4′-тетрахлоразоксибензол XLI [172].
Таким образом последовательность изменения токсичности основных членов ряда галогенированных диоксиновых соединений выглядит следующим образом:
дибензо-n-диоксин > дибензофуран >> бифенил > нафталин
Из табл.12 видно также, что токсичность диоксина I выше или по крайней мере сопоставима с токсичностью таких антихолинэстеразных отравляющих веществ, как табун, зарин, зоман и VX-газ [809,814,815]. Таким образом, утверждение [170,791], что диоксин I — самое токсичное из веществ, синтезированных человеком, в принципе нельзя считать преувеличением увлеченных исследователей или журналистов, хотя, как уже говорилось, есть и более токсичные соединения этого класса.
Как уже упоминалось, токсичность диоксинов определяется их строением, хотя конкретные представления о связи между структурой ПХДД и ПХДФ и их токсичностью претерпели существенную эволюцию. Одно время считалось, что в рядах хлорорганических соединений ПХДД и ПХДФ наиболее токсичны лишь диоксины, содержащие 4-6 атомов хлора с латеральным фрагментом 2,3,7,8-Cl4.
Схема 10 дает определенное представление об этом процессе.
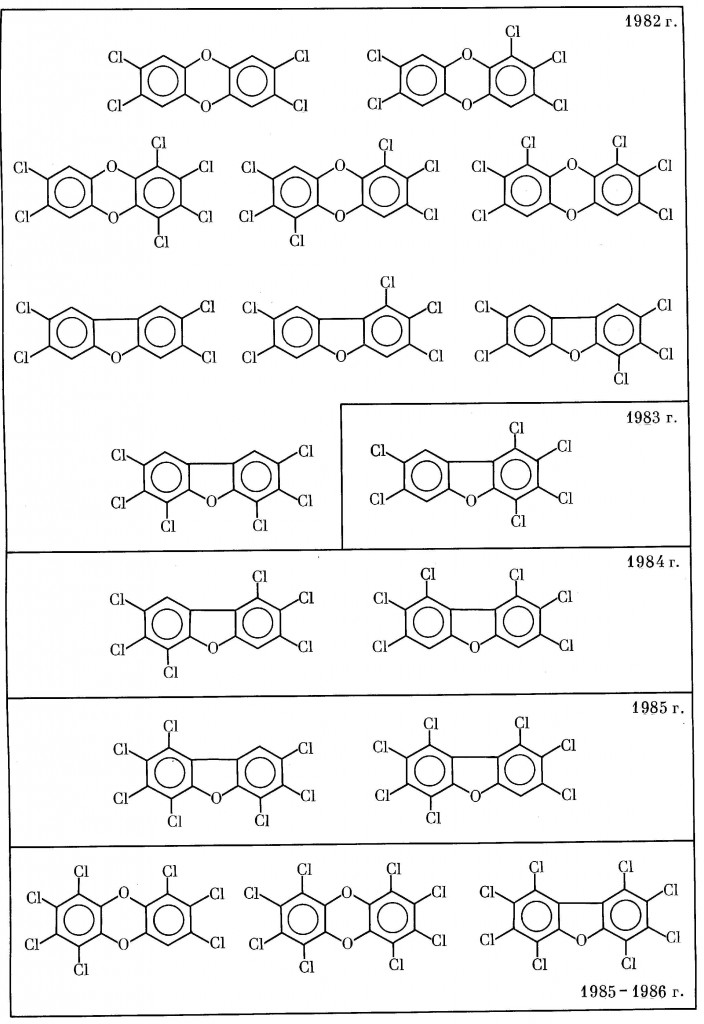
Схема 10. Эволюция представлений о наиболее токсичных ПХДД и ПХДФ
На первой международной конференции «Диоксин-80″ (Рим) в число наиболее токсичных включали 9 соединений [816], а двумя годами позже, на ежегодной конференции Американского химического общества — 10 веществ [166] с 4-6 атомами хлора в латеральном положении. Однако в их число входили все изомеры ГкХДД, но еще не все изомеры ГкХДФ. Примерно к 1983-1984 гг. сформировалось представление о совокупности наиболее токсичных веществ, так называемой «грязной дюжине», которое в наши дни стало общепринятым. В их число включались все без исключения 12 соединений из рядов ПХДД и ПХДФ, обладающих 4-6 атомами хлора, четыре из которых обязательно находятся в латеральных 2,3,7,8-положениях [742,817]. При этом считалось, иногда молчаливо, что не только с понижением, но и с повышением числа атомов хлора токсичность ПХДД и ПХДФ должна снижаться. Опыт, однако, показал, что исключать из рассмотрения гепта- и октахлорированные производные ПХДД и ПХДФ нельзя. В процессе реакций, происходящих в живых организмах, они могут, например, превращаться в более токсичные диоксины. Во всяком случае в отдельных публикациях в число наиболее токсичных стали включать и гептахлоридные производные [818]. Наконец, после токсикологических работ 1985-1986 гг. [146,819], а также сообщения об обнаружении «отсроченной токсичности» ОХДД [807] стало очевидным, что при оценке токсичности диоксинов из поля зрения не должны выпадать ни гепта-, ни октапроизводные.
Таким образом, в число опасных по различным тестам входят не только те диоксины, которые помещены в верхней части схемы 10, но и практически все полигалогенированные соединения, содержащие фрагмент 2,3,7,8-Hal4 [143-147,816]. В результате к 1988 г. сформировалось устойчивое убеждение [57], что все 17 гомологов и изомеров ПХДД и ПХДФ с латеральным структурным мотивом 2,3,7,8-Cl4 — 7 веществ в ряду III и 10 в ряду IV — должны рассматриваться как наиболее токсичные диоксины.
В рядах ПБДД и ПБДФ ситуация аналогична. Таким образом, с учетом токсических характеристик бром- и смешанных хлорброморганических соединений общее число наиболее токсичных диоксинов возрастает до 568 [302]. Действительное положение, однако, еще более сложное. Как оказалось, при наличии 2,3,7,8-Cl4-фрагмента токсичность диоксинов не очень существенно изменяется от дополнительного введения в их скелет некоторых группировок, например NH2, NO2 и т.д. [142].
V.2.2. Хроническая токсичность
Реальное воздействие диоксинов на человека и природу, однако, не адекватно их острой токсичности. Данные последних лет показали, что основная опасность диоксина I и вообще диоксинов III-VIII заключается не столько в их острой токсичноcти, сколько в кумулятивном действии и отдаленных последствиях хронического отравления крайне малыми дозами. Минимальная кумулятивная токсическая доза диоксина I при оральном поступлении в организм человека оценена в 0,1 ppb [820].
Наиболее серьезный фактор воздействия диоксинов на здоровье людей — их влияние на иммунную систему [156-158]. Даже при ничтожных концентрациях они вызывают подавление иммунной системы и нарушают способность организма к адаптации в изменяющихся условиях внешней среды. Это приводит к резкому подавлению умственной и физической работоспособности [158,821].
В несколько более высоких концентрациях диоксины вызывают мутагенный, тератогенный (рождение детей-уродцев от пораженных родителей) и эмбриотоксические эффекты, нарушение жизнедеятельности нервной системы, поражение печени, пищевого тракта и др.
Хотя вопрос о канцерогенной активности диоксинов по отношению к животным давно не вызывает сомнений, данные, касающиеся опасности заболеваний онкологическими болезнями людей, долгие годы представлялись противоречивыми. Еще в конце 70-х годов было обнаружено, что у сельскохозяйственных рабочих, подвергшихся воздействию хлорфенолов и феноксигербицидов, содержавших диоксины, риск заболевания саркомой мягких тканей возрастает в 6 раз [822]. Несколько позже появились многочисленные сообщения о случаях сарком мягких тканей у рабочих, участвовавших в производстве 2,4,5-ТХФ и гербицида 2,4,5-Т и подвергавшихся воздействию диоксина [579,581,588,823-825]. Кроме того, неоднократно сообщалось о статистически значимом увеличении у этих людей частоты злокачественных новообразований различных органов и тканей — желудочно-кишечного и респираторного трактов [581], толстой кишки, носа [826] и т.д. В ряде работ указывается на достаточно четкую корреляцию между воздействием феноксигербицидов и хлорфенолов, с одной стороны, и развитием злокачественных лимфом, с другой [827,828]. Тем не менее до настоящего времени остаются дискуссионными многие вопросы, в частности вопрос о том, являются ли непосредственной причиной канцерогенных эффектов у людей сами феноксигербициды или же переносимыe ими диоксины [829].
Недавно были получены свидетельства того, что 2,3,7,8-ТХДД (I) является прямым канцерогеном для человека [830,831]. Так, в работе [830] подведены итоги многолетнего ретроспективного изучения смертности среди рабочих США, пораженных диоксином I. Всего было обследовано более 5000 рабочих с 12 предприятий, причем исследовали не только медицинские записи о состоянии здоровья рабочих за несколько десятилетий, но и определяли диоксин непосредственно в их организме. Оказалось, что если в целом вопрос о смертности от рака этой группы рабочих еще остается в сфере дискуссии, то для рабочих, имевших контакт с диоксином более 1 года, результаты вполне определенные. В этой последней подгруппе было найдено статистически значимое повышение риска смерти от некоторых форм рака. Тот же вывод следует из обследования, выполненного в Германии среди более 1500 рабочих, которые были заняты на предприятиях по производству гербицидов [831]. В этом случае также было обнаружено статистически значимое повышение вероятности смертности от рака для рабочих, имевших длительный профессиональный контакт с диоксином. Очевидно, что при обследовании рабочих Уфимского ПО «Химпром» и Чапаевского завода химических удобрений, если это будет сделано аналогичным образом, могут быть получены близкие выводы.
Картина мощного и многостороннего воздействия 2,3,7,8-ТХДД и вообще диоксинов на животных и человека, в том числе с учетом порождаемых этим явлением многочисленных научно-технических и социальных последствий, обобщена в работе [95]. В ней даны результаты собственных исследований авторов, а также многочисленные данные изучения биологической активности и токсических эффектов, полученных в ведущих лабораториях мира. Некоторые из выводов [95] можно сформулировать следующим образом.
1. Как яд диоксин наиболее опасен при кумулятивном отравлении малыми дозами. Как уже упоминалось, это связано с тем, что диоксин вызывает последовательное накопление в клетках и тканях биологических мишеней, чрезвычайно специфичных к нему самому. Соответственно в процессе аккумуляции диоксина каждая его новая порция оказывается токсичнее предыдущей. На эту, чисто токсикологическую, особенность накладывается и социальный фон. Картина отравления малыми дозами диоксинов, много более эффективного по сравнению с острым, особенно опасна для стран с «грязными» технологиями производства и использования продукции. В них из-за отсутствия какого-либо контроля со стороны официальных органов данные о поступлении диоксинов в живые организмы с пищей, воздухом и водой просто отсутствуют. Как следствие, результат может оказаться выявленным лишь в виде данных о здоровье популяции на поздней стадии массового отравления, когда что-либо предпринять практически невозможно.
2. Стимулируя образование биологических мишеней, способствуя накоплению в клетках соответствующих М-РНК, диоксины как бы закрепляют появляющийся отрицательный признак. В данном случае это упоминавшиеся выше аномально высокие активности цитохрома Р-450 1А1 и аналогичных гемопротеидов. Особенно чувствительны к диоксину именно те ткани, органы, целые организмы, чье интенсивное развитие совпадает с воздействием токсического фона, т.е. новые организмы — от эмбриона до молодых особей. Отсюда социальный результат — резкое ослабление состояния здоровья молодой части любой популяции.
3. Не обладая генотоксическим действием, диоксины не поражают генетический материал клеток организмов непосредственно. Тем не менее они особенно эффективно поражают именно генофонд аэробных популяций, поскольку именно они разрушают общий механизм защиты генофонда от воздействия внешней среды. Условия среды могут резко усилить мутагенное, эмбриотоксичное и тератогенное действие.
4. Еще одно воздействие генетического плана заключается в том, что диоксины разрушают механизм адаптации аэробных организмов к внешней среде. Как следствие возрастает их чувствительность к различного рода стрессам и к многочисленным химическим веществам, являющимся постоянными спутниками организмов в современной цивилизации. Последний аспект практически является двусторонним: синергисты диоксинов усиливают их собственное токсическое действие, а диоксины в свою очередь провоцируют токсичность ряда нетоксичных веществ. Социальное следствие этой и предшествующих особенностей диоксиновых интоксикаций — последовательное и малоконтролируемое ухудшение генетического здоровья пораженных популяций.
5. Для токсического действия диоксинов характерен длительный период скрытого действия. Кроме того, признаки диоксиновой интоксикации очень многообразны и в значительной степени определяются на первый взгляд привходящими обстоятельствами, т.е. зависят не только от дозы яда и способа его введения, но также от видовых, возрастных и индивидуальных особенностей пораженного организма. В социальном плане эта особенность особенно важна, поскольку выдвигает большие требования к квалификации санитарно-эпидемиологических служб.
V.2.3. Коэффициент токсичности. Диоксиновый эквивалент
Многообразие смесей диоксинов, реально существующих в природе, а также неравноценность токсического действия каждого из них не позволяют строго оценивать действительную опасность этих ядов для конкретных объектов и регионов. В связи с этим при работе со смесями оперируют приведенными величинами. Другими словами, токсичность каждого диоксина, главным образом рядов III-VIII, приводят к единому эталону, в качестве которого избран самый токсичный — 2,3,7,8-ТХДД (I) [817,832,833].
Для каждого диоксина из рассматриваемых рядов (пока главным образом из рядов III и IV) находят коэффициент токсичности (КТ) относительно диоксина I. Его определяют несколькими способами на основе имеющихся токсикологических и биологических данных, что существенно повышает надежность всей концепции:
- по величинам LD50, характеризующим острую токсичность диоксинов [817];
- по индукции арилуглеводородгидроксилазы (АНН) [18,19,834,835] и других энзимов;
- по канцерогенному эффекту [832];
- по совокупности одновременно нескольких эффектов [15,17,833] и т.д.[4,24].
Система КТ позволяет приводить к токсическому эквиваленту (диоксиновому эквиваленту, ДЭ) токсические характеристики любой реальной смеси диоксинов, если предварительно определено содержание в ней каждого действующего компонента. Другими словами, токсичность сложной смеси ПХДД и ПХДФ может быть выражена через токсичность 2,3,7,8-ТХДД (I), взятого в эквивалентном по токсичности количестве (в весовых количествах I).
Система ДЭ исходит из традиционного предположения об аддитивности токсического действия отдельных диоксинов в сложных смесях ПХДД и ПХДФ [21,233,836]. Эта предпосылка справедлива, однако, далеко не всегда. Во всяком случае необходимость учета синергических (см., например, [233,837]) и уже упоминавшихся антагонистических [307,381,838] эффектов становится для ПХДД и ПХДФ практической задачей. Очевидно, то же самое следует учитывать и при распространении системы ДЭ на наиболее токсичные ПХБ [839].
Впервые идея использования КТ была предложена в 1977 г. [148,833]. Хотя не все заложенные посылки (табл.13) получили в последующем подтверждение, сама идея [833] как способ оценки суммарной токсичности сложных смесей диоксинов носила принципиальный характер. Вcкоре было создано несколько национальных систем КТ, нашедших практическое применение [4,15,19,21,24,817,832,834,835], причем система, предложенная в 1982-1983 гг. одной из групп США [817] и обновленная в 1986 г. [840], одно время особенно широко использовалась во многих странах. Нашли применение в своих странах и другие системы КТ, разработанные специалистами Канады [15], Швейцарии [19,841], Германии [21].
В последние годы созданы системы КТ, ставшие в международном сообществе особенно популярными. Одна из них рекомендована Агентством охраны природы США (EPA) [6], а две другие созданы группой ученых северных стран Европы (система NORDIC, 1988 г. [24]), а также международной группой специалистов [56,57]. В табл.13 приведено обобщение некоторых систем КТ из числа наиболее ранних и самых последних (см. также [56,832]).
Системы коэффициентов токсичности (КТ) хлорорганических
диоксинов ПХДД и ПХДФ относительно 2,3,7,8-ТХДД (I)
| Группа изомеров | Изомеры | Коэффициент токсичности | |||||||
| 1977 [833] | Канада 1982 [15] | США 1983 [817] | EPA США 1987 [6] | Германия 1985 [21] | Швейцария 1987 [104,841] | NORDIC 1988 [24] | Международная 1988 [56] | ||
| III (ПХДД) | |||||||||
| Cl4 | 2,3,7,8 | 1 | 1 | 1 | 1 | 1 | 1 | 1 | 1 |
| . | Остальные | 1 | 0,01 | 0 | 0,01 | 0,01 | 0 | 0 | 0 |
| Cl5 | 1,2,3,7,8 | 0,1 | 1 | 1 | 0,5 | 0,1 | 0,4 | 0,5 | 0,5 |
| . | Остальные | 0,1 | 0,01 | 0 | 0,005 | 0,01 | 0 | 0 | 0 |
| Cl6 | 1,2,3,4,7,8 | 0,1 | 1 | 0,03 | 0,04 | 0,1 | 0,1 | 0,1 | 0,1 |
| . | 1,2,3,6,7,8 | 0,1 | 1 | 0,03 | 0,04 | 0,1 | 0,1 | 0,1 | 0,1 |
| . | 1,2,3,7,8,9 | 0,1 | 1 | 0,03 | 0,04 | 0,1 | 0,1 | 0,1 | 0,1 |
| . | Остальные | 0,1 | 0,01 | 0 | 0,0004 | 0,01 | 0 | 0 | 0 |
| Cl7 | 1,2,3,4,6,7,8 | 0,1 | 1 | 0 | 0,001 | 0,01 | 0,01 | 0,01 | 0,01 |
| . | Другой | 0,1 | 0,01 | 0 | 0,00001 | 0,001 | 0,01 | 0 | 0 |
| Cl8 | - | 0 | 0 | 0 | 0 | 0,001 | 0,001 | 0,001 | 0,001 |
| IV (ПХДФ) | |||||||||
| Cl4 | 2,3,7,8 | 0,1 | 0,02 | 0,33 | 0,1 | 0,1 | 0,1 | 0,1 | 0,1 |
| . | Остальные | 0,1 | 0,0002 | 0 | 0,001 | 0,01 | 0 | 0 | 0 |
| Cl5 | 1,2,3,7,8 | 0,1 | 0,02 | 0,33 | 0,1 | 0,1 | 0,01 | 0,01 | 0,05 |
| . | 2,3,4,7,8 | 0,1 | 0,02 | 0,33 | 0,1 | 0,1 | 0,4 | 0,5 | 0,5 |
| . | Остальные | 0,1 | 0,0002 | 0 | 0,001 | 0,001 | 0 | 0 | 0 |
| Cl6 | 1,2,3,4,7,8 | 0,1 | 0,02 | 0,01 | 0,01 | 0,1 | 0,1 | 0,1 | 0,1 |
| . | 1,2,3,6,7,8 | 0,1 | 0,02 | 0,01 | 0,01 | 0,1 | 0,1 | 0,1 | 0,1 |
| . | 2,3,4,6,7,8 | 0,1 | 0,02 | 0,01 | 0,01 | 0,1 | 0,1 | 0,1 | 0,1 |
| . | 1,2,3,7,8,9 | 0,1 | 0,02 | 0,01 | 0,01 | 0,1 | 0,1 | 0,1 | 0,1 |
| . | Остальные | 0,1 | 0,0002 | 0 | 0,0001 | 0,01 | 0 | 0 | 0 |
| Cl7 | 1,2,3,4,6,7,8, | 0,1 | 0,12 | 0 | 0,001 | 0,01 | 0,01 | 0,01 | 0,01 |
| . | 1,2,3,4,7,8,9 | 0,1 | 0,12 | 0 | 0,001 | 0,01 | 0,01 | 0,01 | 0,01 |
| . | Остальные | 0,1 | 0,0002 | 0 | 0,00001 | 0,001 | 0 | 0 | 0 |
| Cl8 | . | 0 | 0 | 0 | 0 | 0,001 | 0 | 0,001 | 0,001 |
Следует подчеркнуть, однако, что сложность задачи и несопоставимость исходных токсикологических посылок не позволили пока разработать единую систему КТ, признанную всеми группами ученых. По-видимому, две недавно предложенные системы КТ, занимающие в табл.13 колонки справа — NORDIC [24] и международная [56,57],- могут считаться наиболее подходящими [842]. Они учитывают новейшие токсикологические данные и различаются лишь в оценке токсичности 1,2,3,7,8-Cl5-ДФ. По-видимому, международная система КТ станет общепринятой. С 1989 г. она используется в Нидерландах [104], а с 5.V.1991 г. признана в бывшем СССР. Помимо простоты пользования, в этих системах учитывается также вклад в токсичность реальных смесей таких диоксинов, как Cl7- и Cl8-ДД и -ДФ. Другими словами, в этих системах КТ уже учитываются все 17 хлорорганических соединений рядов ПХДД и ПХДФ с латеральным фрагментом 2,3,7,8-Cl4, а не только те 12, которые долгое время было принято считать наиболее токсичными.
К международной системе были «привязаны» и КТ, рассчитанные недавно в работе [839] для трех наиболее токсичных ПХБ:
3,4,3′,4′-Cl4 (ПХБ-77) - 0,0021
3,4,5,3′,4′-Cl5 (ПХБ-126) - 0,3
3,4,5,3′,4′,5′-Cl6 (ПХБ-169) - 0,0012
Эти расчеты опирались на данные [146] по индукции арилуглеводородгидроксилазы, вызываемой этими изомерами ПХБ.
Рассматриваемые системы КТ далеки, однако, от совершенства и, несомненно, потребуют дополнения и развития [145].
В частности, в международных системах [24,55] пока не предусматривается учет вклада в токсичность смесей целых групп изомеров (Cl4-, Cl5-, Cl6- и Cl7-ДД и -ДФ), не содержащих фрагмента 2,3,7,8-Cl4. Хотя эта особенность исходит из очевидной необходимости упрощения шкал КТ, она не может не занижать реальной опасности смесей диоксинов для человека. В системах КТ, используемых в США [6] и Германии [21], токсичность не 2,3,7,8-изомеров учитывается. Действующие шкалы КТ не учитывают также тот факт, что переход диоксинов из объектов окружающей среды в организм высших представителей фауны (рыба, человек и другие млекопитающие) происходит токсикологически ориентированно и сопровождается аккумулированием главным образом 2,3,7,8-Hal4-содержащих веществ, причем для разных организмов в разной степени [223,264,843] (разд.VII.2). Соответственно при оценке токсичности на основе лишь измерений диоксинов, выполненных в воде, воздухе и почве, опасность при расчете ДЭ, по существу, занижается, поскольку расчеты не учитывают индивидуальных и групповых особенностей живых организмов. Система КТ не включает в себя далее возможности превращений диоксинов, происходящих непосредственно в живых организмах, когда менее токсичные соединения могут превращаться в более токсичные. Эта система не учитывает также того факта, что диоксины, наряду с прямым действием, обладают также синергическим, усиливая токсическое действие других веществ. Нельзя, наконец, исключить вероятность того, что при практических исследованиях могут встретиться задачи, которые потребуют учета токсического вклада других, не учтенных пока факторов.
В целом системы КТ, разработанные различными токсикологическими школами, довольно близки (табл.13). Соответcтвенно, не очень различаются и даваемые с их помощью (в виде ДЭ) оценки степени загрязнения. В частности, разброс в расчетах, выполненных в работе [275] при оценке токсичности микровыбросов одной из шведских МСП с помощью четырех систем КТ 1986-1988 гг., не превысил 10%. Наибольшие различия возникают для высокохлорированных диоксинов. Однако сам подход к оценке относительной токсичности различных диоксинов пока еще остается в сфере критического анализа [6,844].
Практическая работа по оценке загрязненности объектов реальными смесями ПХДД и ПХДФ включает два этапа — аналитический и токсикологический. Первый этап предусматривает раздельное определение в образце каждого компонента смеси. На последующем этапе оценивается степень опасности всей смеси (в ДЭ) путем суммирования ее компонент с учетом КТ каждого. В итоге для конкретной смеси диоксинов находится ДЭ, выражаемый в весовых единицах наиболее токсичного 2,3,7,8-ТХДД (I).
| « Назад | Оглавление | Вперед » |